2C-E
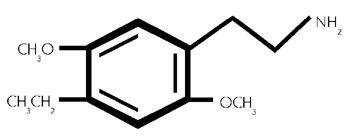
Formel aus:
(42/515)
Andere Namen:
2,5-Dimethoxy -4- ethylphenethylamin. (42/515)
Allgemeines:
Dieses Halluzinogen ist ein Phenethylamin. Es ist damit nahe verwandt mit 2C-B, Meskalin, oder auch 2C-C. Es unterscheidet sich chemisch von letzterem nur durch einen anderen Substituenten an der 4. Position des aromatischen Benzolringes. 2C-B hat an dieser Stelle zum Beispiel ein Bromatom, 2C-C ein Chloratom und 2C-E eine Ethylgruppe. (eigen)
Haengt man bei einem Phenethylamin noch eine Methylgruppe an der Ethylaminseitengruppe an, kommt man zu der Gruppe der Amphetamine. Grundsaetzlich scheint die Regel zu gelten, dass wenn ein Phenethylamin psychoaktiv ist, ist auch sein Amphetamingegenstueck wirksam ist. Mehr noch, es ist sogar allgemein staerker. (eigen)
Das Amphetaminhomolog des Halluzinogens 2C-E ist nun DOET, dass nicht nur laenger wirkt, sondern auch betraechtlich staerker, wie der amerikanische Drogenforscher und -designer Alexander Shulgin in seinem Buch "PHIKAL" bemerkt. In diesem Fall (2C-E und DOET) kann die obige These bestaetigt werden. (42/518)
A. Shulgin gibt in seinem Buch "PHIKAL" folgende allgemeinen Bemerkungen zum Halluzinogen 2C-E an:
Der Dosisbereich ist zweckmaessig breit. Mit 10 mg hat es einige ziemlich reiche +++ Erfahrungen gegeben, und ich habe den Bericht von einer jungen Dame von einem 30 mg Versuch gehabt, der sehr erschreckend war. Einige Leute haben ueber 2C-E gesagt, 'Ich glaube nicht, dass ich es mag, weil es nicht so spassig ist. Aber ich beabsichtige es wieder zu untersuchen.' Es gibt etwas hier, dass den Experimentator belohnen wird. Eines Tages wird der volle Charakter von 2C-E verstanden werden, aber im Moment, laesst man es als schwieriges und lohnendes Material ruhen. (42/518)
Dosis:
A. Shulgin, der Verfasser von "PHIKAL", dem Standardwerk ueber halluzinogene Phenethylamine und Amphetamine, gibt einen Dosisbereich von 10-25 mg an, indem die Droge halluzinogen wirkt. (42/517)
Wirkdauer:
Die Dauer der Wirkung wird mit 8-12h von A. Shulgin in seinem Werk "PHIKAL" angegeben. (42/517)
Wirkungen:
Alexander Shulgin verfasste das Buch "PHIKAL", welches zum Standardwerk der halluzinogenen Forschung ueber halluzinogene Phenethylamine und Amphetamine wurde. In diesem Werk gibt der bekannte Drogenforscher folgende subjektive Wirkberichte an:
20 mg: Der Blick aus dem Fenster war unwirklich. Der Garten war wie auf das Fenster gemalt, und jedes Blumenblatt und jeder Grasbusch und jedes Blatt eines Baumes war vorsichtig aus feinen Strichen mit Oelfarbe auf der Oberflaeche des Glases geformt. Es war nicht dort aussen; es war hier vor mir. Die Frau, die die Pflanzen goss, war komplett unbeweglich, wie durch Vermeer bewegungsunfaehig gemacht. Als ich wieder nachsah, war sie an einem anderen Platz, aber wiederum unbeweglich. Mir war es bestimmt ein ewiger Museumsbesucher zu werden. (42/517f.)
25 mg: Nach Minuten war ich aengstlich und schweissnass. Jede Person hat seine eigene Art der toxischen Psychose, meine beginnt immer mit Stimmen in meinem Kopf, die zu mir sprechen, ueber alle meine schlimmsten Aengste, ein Haufen Warnungen und tiefe Aengste. 20 Min. spaeter verging dieses komplexe Chaos, so schnell wie es gekommen war. Mit niederen Dosen war 2C-E ein wirklich erfreulicher Aesthetiksteigerer. Aber es hat wirklich eine steile Dosis/Reaktionskurve. (42/517f.)
Sucht:
Die Ausbildung einer koerperlichen Abhaengigkeit ist nicht bekannt. (eigen)
Synthese:
A. Shulgin gibt in seinem Buch "PHIKAL" folgendes Herstellungsverfahren an:
Eine Suspension von 140g wasserfreiem AlCl3 in 400 ml CH2Cl2 wurde mit 100g Acetylchlorid versetzt. Diese Masse wurde zu einer kraeftig geruehrten Loesung von 110g p-Dimethoxybenzol in 300 ml CH2Cl2 hinzugefuegt. Ruehren wurde bei Umgebungstemperaturen fuer zusaetzliche 40 Min. fortgesetzt. Dann wurde alles in 1l Wasser gegossen und die Phasen getrennt. Die waessrige Phase wurde mit 2x100 ml CH2Cl2 extrahiert. Die vereinigten organischen Phasen wurden mit 3x150 ml 5%-iger NaOH gewaschen. Diese Waschungen wurden, nach Vereinigung und Ansaeuerung, mit 3x75ml CH2Cl2 extrahiert. Die Extrakte wurden 1x mit gesaettigter NaHCO3 Loesung gewaschen. Entfernen des Loesungsmittels im Vakuum ergab 28.3 g 2-Hydroxy-5-methoxyaceto-phenon, als gelbe Kristalle. Nach dem Umkristallisieren aus 2 Volumen kochendem MeOH und Lufttrocknen wurden 21.3 g Produkt mit einem mp von 49-49.5 Grad Celsius erhalten. Die CH2Cl2 Fraktion der Waschung mit der Base, oben, wurde vom Loesungsmittel im Rotationsverdampfer befreit, um restliches Oel zu ergeben, dass beim Destillieren bei 147-150 Grad Celsius an der Wasserstrahlpumpe 111.6 g 2,5-Dimethoxyacetophenon ergab, als beinahe weisses Oel.
In einem rundboedigen Kolben, ausgeruestet mit einem Rueckflusskuehler, einem abhebbaren Adapter, einem Eintauchthermometer und einem magnetischen Ruehrer, wurden 100g 2,5-Dimethoxyacetophenon, 71g 85%-ige KOH Plaetzchen, 500 ml Triethylenglycol und 125ml 65%-iges Hydrazin gegeben. Die Mischung wurde zum Sieden durch Erhitzen mit einem elektrischen Mantel gebracht. Das Destillat wurde entfernt. Man liess die Temperatur der Kolbeninhaltsstoffe unaufhoerlich steigen. Als die Kolbentemperatur 210 Grad Celsius erreicht hatte, wurde ein Rueckfluss etabliert und fuer zusaetzliche 3h gehalten. Nach Abkuehlen wurden die Reaktionsmischung und das Destillat vereinigt, in 3l Wasser gegossen, und mit 3x100 ml Hexan extrahiert. Nach Waschen der vereinigten Extrakte mit H2O, wurde das Loesungsmittel entfernt, was 22g blass strohfarbene Fluessigkeit ergab, die frei war von beiden Hydroxy und Carbonylgruppen, festgestellt durch Infrarot. Dies wurde bei 120-140 Grad Celsius an der Wasserstrahlpumpe destilliert, um 2,5-Dimethoxy-1-ethylbenzol, als weisses Fluessigprodukt, zu ergeben. Ansaeuern der verbrauchten, waessrigen Phase mit konzentrierter HCl erzeugte ein schweres schwarzes Oel, welches mit 3x100 ml CH2Cl2 extrahiert wurde. Entfernen des Loesungsmittels im Rotationsverdampfer ergab 78g schwarzen Rest, der bei 90-105 Grad Celsius mit einem Druck von 0.5 mm/Hg destilliert wurde, um 67.4 g orange-bernsteinfarbenes Oel zu ergeben, dass hauptsaechlich 2-Ethyl-4-methoxyphenol war. Dieses Material koennte eventuell als Startmaterial fuer Ethoxyhomologe gebraucht werden. Jedoch ergab Remethylierung (mit CH3I und KOH in MeOH) zusaetzliche 28g 2,5-Dimethoxyethylbenzol.
Eine Loesung von 8.16g 2,5-Dimethoxy-1-ethylbenzol in 30 ml CH2Cl2 wurde mit gutem Ruehren auf 0 Grad Celsius abgekuehlt und unter eine Inertatmosphaere aus He gegeben. Es wurden dann 11.7ml wasserfreies Zinnchlorid hinzugefuegt, gefolgt von 3.95ml Dichlormethyl-methyl-ether, tropfenweise, verteilt auf eine 0,5h. Die geruehte Reaktionsmischung liess man auf Zimmertemperatur erwaermen. Dann wurde sie 1h lang auf dem Dampfbad gehalten. Die Reaktionsmischung wurde in 1l H2O gegossen, mit 3x75ml CH2Cl2 extrahiert, und die vereinten Extrakte mit verd. HCl gewaschen. Die organische Phase wurde verdunstet im Vakuum, was 10.8g dunkles viskoses Oel ergab. Dies wurde bei 90-110 Grad Celsius mit einem Druck von 0.2mm/Hg destilliert, um farbloses Oel zu ergeben, dass beim Kuehlen weisse Kristalle bildete. Die Ausbeute an 2,5-Dimethoxy-4-ethylbenzaldehyd war 5.9g Material, dass einen mp von 46-47 Grad Celsius hatte. Nach Reinigung durch den Bisulfitkomplex, erhoehte sich der mp auf 47-48 Grad Celsius. Der Gebrauch der Vilsmeier'schen Aldehydsynthese (mit POCl3 und N-Methylformanilid) ergab Ergebnisse, die total unvorhersagbar waren. Das Malononitrilderivat (aus 0.3g von diesem Aldehyd und 0.3g Malononitril in 5ml EtOH und einem Tropfen Triethylamin) bildete rote Kristalle, welche nach dem Umkristallisieren aus Toluol, einen mp von 123-124 Grad Celsius hatten.
Eine Loesung von 21g des nicht-umkristallisierten 2,5-Dimethoxy-4-ethylbenzaldehyds in 75g Nitromethan wurde mit 4g wasserfreiem Ammoniumacetat versetzt und auf dem Dampfbad rund 2h lang erhitzt. Der Fortschritt der Reaktion wird am besten durch TLC Analyse der rohen Reaktionsmischung auf Kieselerde Gel Platten mit CH2Cl2 als Entwicklerloesungsmittel verfolgt. Die ueberschuessigen Loesungsmittel/Reagenzien wurden im Vakuum entfernt, was koernige orange Feststoffe ergab, die aus 7 Volumen kochendem MeOH umkristallisiert wurden. Nach 1h Kuehlen mit aeusserem Eiswasser, wurde das gelbe, kristalline Produkt durch Filtration entfernt, mit kaltem MeOH gewaschen und an der Luft getrocknet, um 13.4g 2,5-Dimethoxy-4-ethyl-beta-nitrostyren zu ergeben. Der mp war 96-98 Grad Celsius, der auf 99-100 Grad Celsius, nach einer zweiten Umkristallisierung aus MeOH, gehoben wurde.
Eine Gesamtmenge von 120 ml einer 1M Loesung von LAH in THF (120 ml der 1M) wurde in einen 3-Hals 500 ml Kolben gegeben, und unter einer Inertatmosphaere mit gutem magnetischem Ruehren gebracht. Diese Loesung wurde auf 0 Grad Celsius mit einem aeusseren Eiswasserbad abgekuehlt. Es wurden dann 3ml 100%-ige H2SO4 hinzugefuegt, verteilt auf 0,5h. Dies wurde von einer Loesung von 5.85g 2,5-Dimethoxy-4-ethyl-beta-nitrostyren gefolgt, in 40 ml warmen THF. Die Reaktionsmischung wurde eine 0,5h lang geruehrt, auf Zimmertemperatur gebracht, auf dem Dampfbad 0,5h lang erhitzt. Man liess die Mischung auf Zimmertemperatur zurueckkehren. Die tropfenweise Addition von IPA zerstoerte das ueberschuessige Hydrid. Etwa 4.5ml 5%-ige NaOH erzeugten einen weissen Huettenkaese, in einem basischen, organischen Medium. Diese Mischung wurde filtriert, und mit THF gewaschen. Das Filtrat wurde verdampft, um 2.8g beinahe weisses Oel zu erzeugen. Der Filterkuchen wurde in THF resuspendiert, mit zusaetzlichen 15ml 5%-iger NaOH basischer gemacht, und wieder filtriert. Das Filtrat wurde entfernt, um zusaetzliche 2.8g Rohprodukt zu erzeugen. Diese Reste wurden vereinigt und bei 90-100 Grad Celsius mit einem Druck von 0.25mm/Hg destilliert, um ein farbloses Oel zu ergeben. Dieses wurde in 30 ml IPA geloest, mit konz. HCl neutralisiert, und mit 50 ml wasserfreiem Et2O verduennt, um 3.87g 2C-E-HCl, als praechtige weisse Kristalle, zu ergeben, nach ploetzlicher Kristallisation, Filtration, Waschen mit Et2O und Lufttrocknen. Eine aehnliche Ausbeute kann durch Reduktion von Nitrostyren in einer Suspension von LAH in THF erhalten werden, ohne Gebrauch von H2SO4. 11.3g LAH in 300 ml trockenen THF wurden tropfenweise zu einer Loesung von 13.4g 2,5-Dimethoxy-4-ethyl-beta-nitrostyren in 75ml THF hinzugefuegt, verteilt auf 2h. Die Mischung wurde am Rueckfluss zusaetzliche 8h gehalten, und durch die vorsichtige Addition von 11ml H2O beendet, gefolgt von 11ml 15%-iger NaOH, und schliesslich anderen 33ml H2O. Diese Masse wurde filtriert, mit THF gewaschen, und die vereinten Filtrate und Waschungen zu einem Rest im Vakuum verdampft. Die annaehernd 15ml Rest wurden in 300 ml CH2Cl2 geloest und mit 200 ml H2O versetzt, die 20 ml konz. HCl beinhalteten. Beim Schuetteln der Mischung lagerte sich eine Masse Hydrochloridsalz ab, welches mit einer Quantitaet zusaetzlichem H2O verduennt wurde. Die organische Phase wurde mit zusaetzlicher verd. HCl extrahiert. Diese waessrigen Phasen wurden vereint. Nachdem diese mit 25%-iger NaOH basisch gemacht worden waren, wurde diese Phase wieder mit 3x75ml CH2Cl2 extrahiert. Nach Entfernen des Loesungsmittels wurden 12.6g farbloses Oel erhalten. Dies wurde in 75ml IPA geloest und mit konz. HCl neutralisiert. Die verfestigte Masse, die sich bildete, wurde mit zusaetzlichen 50 ml IPA gelockert, und dann filtriert. Nach Et2O Waschen und Lufttrocknen wurden 7.7g 2C-E-HCl erhalten, als glaenzende weisse Kristalle. Anal. (C12H20ClNO2) C,H. (42/515ff.)