DPT
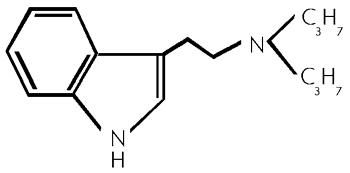
Formel aus:
(62)
Andere Namen:
Dipropyltryptamin, 3- [2- (dipropylamino) ethyl] -indol, N,N -Dipropyltryptamin. (62)
Dosis:
Die Droge kann injiziert oder inhaliert werden. Die optimale, fuer therapeutisch Einsaetze eingesetzte Dosis betraegt 75-150 mg. (25, 38) Es wurde stets i.m. gegeben, da es p.o. unwirksam ist. (38) J. Ott empfiehlt eine Dosis von 1 mg/kg. (62) P.o. unwirksame Tryptamine koennen durch die vorherige Aufnahme eines MAO-Hemmers, dennoch durch den Magen aufgenommen werden. Demnach ist es moeglich, DPT oral aktiv zu machen, indem man einen MAO-Hemmer zuvor einnimmt, der verhindert dass die Substanz im Magen abgebaut wird. Stattdessen wird Sie dann in den Wirkort im Gehirn transportiert. (eigen)
Spezifikation:
Die Summenformel lautet C16H24N2. Das Mol. Gew. betraegt 244,38. DPT bildet Hydrochloridkristalle mit einem mp von 174,5-178 Grad Celsius und ist loesl. in H2O. (62)
Allgemeines:
Es ist eine synthetische Droge, (62) und ein typisches, halluzinogenes Tryptamin. Es ist damit auch nahe verwandt mit den Pilzhalluzinogenen Psilocin, Baeocystin und Psilocybin, welche ebenfalls Tryptamine sind. Es ist aber auch mit DMT (Dimethyltryptamin), einer im Pflanzenreich weitverbreiteten, halluzinogenen Rauschdroge, strukturell verwandt. (eigen)
Nach dem Verbot von LSD, auch fuer den psychotherapeutischen Einsatz, wurde es vermehrt als Ersatz eingesetzt. Es wurde systematisch in seiner Funktion als Zusatz zur Psychotherapie von Alkoholikern und Krebspatienten erforscht, und erwies sich in seiner Wirkung vergleichbar mit LSD (Grof et al., 1973; Richards et al., 1979) (25) Die Ergebnisse der DPT-Studie hat William A. Richards, ein Psychologe und Therapeut am Maryland Psychiatric Research Center, der seit 1967 an dem Krebsprogramm mitarbeitete, beschrieben und kritisch bewertet. (38)
Wirkungen:
Die Wirkung setzte sofort ein, da die Droge meistens i.m. appliziert wurde, (38) und die Wirkungen sind aehnlich wie beim verwandten DMT. (13) An dieser Stelle muss auch auf die Beschreibung von DMT und DET verwiesen werden, wo sich genauere Ausfuehrungen befinden. (eigen)
Sucht:
Die Ausbildung einer koerperlichen oder glaubhaften psychischen Abhaengigkeit ist nicht bekannt. (eigen)
Synthese:
Michael Valentine Smith gibt in seinem Werk "Psychedelic Chemistry", dass lange Zeit als Zusammenfassung bestehender wissenschaftlicher Literatur in diesem Bereich der Drogenforschung gedient hat, folgendes Verfahren an, welches aus seinem Buch "Psychedelic Chemistry" entnommen wurde und eigentlich zur Herstellung von DET geeignet ist: Es spricht einiges gegen diese Beschreibung, denn Sie ist zu wenig praezise und laesst sich anhand des Buches, dass ich habe nicht ausreichend belegen...
- 5,5g Indol und 15ml Cyclohexan werden zu 0,5g feinpulversiertem Kupfer gegeben. Es wird am Rueckfluss gekocht und tropfenweise 2,9g Diazoaceton dazugefuegt. Nach einer bestimmten Zeit laeuft die Reaktion sehr schnell ab und bildet 2 Schichten aus. Es wird filtriert und im Exsikkator (unter Vakuum) verdunstet oder destilliert, um 2,6g 3-Indolyl-aceton zu bekommen.
- 3,3g3-Indolyl-aceton werden in 100 ml EtOH gegeben. Es wird ueber einen Palladium-Karbon Katalysator in Gegenwart von 0,04M DPA reduziert. Nach 2h wird filtriert und im Exsikkator verdampft, um DPT zu bekommen. (23)
"(von Tryptamin aus): Eine Loesung von 1,6g Tryptaminbase in 10 ml IPA wurde mit 5,1g Propyliodid und 5,2g Diisopropylethylamin behandelt und 36h bei Raumtemperatur geruehrt. Die leicht fluechtigen Stoffe wurden unter Vakuum entfernt, und der Rest wurde zwischen CH2Cl2 und H2O, welches mit NaOH basisch gemacht wurde, aufgeteilt. Die organische Phase wurde abgetrennt. Die waessrige Phase wurde mit 2 zusaetzlichen Portionen CH2Cl2 extrahiert und die vereinten Extrakte wurden von den Loesungsmitteln im Vakuum befreit. Der Rest, ein fluessiges, braunes Oel, dass 2,75g wog, wurde mit 5g Essigsaeureanhydrid behandelt und am Dampfbad 20 Minuten erhitzt. Nach dem Abkuehlen, wurde eine kleine Menge an Ammoniumhydroxid hinzugefuegt und die Mischung wurde in 200 ml 0,5N H2SO4 gegeben. Die waessrige Loesung wurde 3x mit CH2Cl2 gewaschen und anschliessend mit 25%-iger NaOH basisch gemacht. Diese Loesung wurde mit 3x40 ml CH2Cl2 extrahiert, die Extrakte vereint, und das Loesungsmittel im Vakuum entfernt. Der oelige Rest wurde bei 145-155 Grad Celsius bei 0,08 mm/Hg destilliert, um 1,14g N,N-Dipropyltryptaminbase, als weisses Oel zu ergeben. Dieses wurde in 5ml IPA geloest, mit konz. HCl angesaeuert und mit 20 ml wasserfreiem Et2O verduennt, um DPT in Form eines weissen Pulvers zu ergeben. Die Ausbeute betrug 1,10g (39%) mit einem mp von 174-176 Grad Celsius. Der IR (in cm-1): 759, 774, 831, 987 (br.), 1084, 1101. Der Austausch der organischen Base Diisopropylethylamin mit einer gleichmolaren Menge an NaHCO3 ergab den gleichen Stoff, aber mit einer Ausbeute, die geringer als 10% war."
A. Shulgin fuehrt noch eine weitere Synthese in seinem Werk an:
"(von Indol): Zu einer gut geruehrten Loesung von 10g Indol in 150 ml wasserfreiem Et2O wurde tropfenweise, verteilt auf die Dauer von 30 Min., eine Loesung von 11g Oxalylchlorid in 150 ml wasserfreiem Et2O hinzugefuegt. Das Ruehren wurde zusaetzliche 15 Min. fortgesetzt, waehrend dieser Zeit trennte sich das Indol-3-ylglyoxylchlorid ab. Dieses Zwischenprodukt wurde durch Filtration entfernt, und sofort im naechsten Reaktionsschritt eingesetzt. Die Substanz wurde in kleinen Portionen zu 20 ml wasserfreiem Dipropylamin hinzugefuegt, welches geruehrt wurde. Es wurde dann ein Ueberschuss von 2N HCl hinzugefuegt, die Mischung abgekuehlt, und die restlichen Feststoffe durch Filtration entfernt. Diese wurden aus waessrigen EtOH umkristallisiert, um - nach dem Luftrocknen - 13,2g Indol-3-yl-N,N-dimpropylglyoxylamid mit einem mp von 95-96 Grad Celsius zu ergeben. Eine Loesung von 13g dieses Stoffes in 350 ml wasserfreiem Dioxan wurde langsam zu 19g LAH in 350 ml Dioxan hinzugefuegt, welches gut geruehrt und am Rueckfluss gehalten wurde unter einer Inertathmosphaere. Nachdem die Addition komplett war, wurde das Kochen am Rueckfluss fuer zusaetzliche 16h aufrechterhalten. Die Reaktionsmischung wurde abgekuehlt und das ueberschuessige Hydrid wurde durch Filtration entfernt, mit heissem Dioxan gewaschen und die Filtrate und Waschungen wurden kombiniert, getrocknet ueber wasserfreim MgSO4 und das Loesungsmittel im Vakuum entfernt. Der braeunliche Rest wurde in wasserfreiem Et2O geloest und mit wasseerfreiem HCl gesaettigt. Die restlichen Kristalle wurden aus Benzol/MeOH umkristallisiert, um 11,9g (49%) N,N-DPT-HCl mit einem mp von 178-179 Grad Celsius zu ergeben. (101)
Dosis:
A. Shulgin fuehrt in seinem Werk THIKAL einen Dosisbereich von 100-250 mg, oral eingenommen, an. (101/428)
Wirkungsdauer:
Die Wirkung dauert 4-5h. Es folgt eine relativ schnelle Rueckkehr zu einem gewoehnlichen Bewusstseinszustand. (25, 38) Shulgin fuehrt einen eher kuerzeren Wirkungsbereich von 2-4h an. (101/428)
Geschichte:
1954: Synthese durch Speeter. (62)
1959: Synthese durch Vitali. (62)
1959: Synthese durch Barlow. (62)